La técnica utiliza las células de la piel del paciente para generar células madre pluripotentes inducidas (CMPi), que son capaces de convertirse en distintos tipos de tejidos, incluyendo células sanguíneas maduras. Los científicos afirman que su método, que repara el gen beta-globina (HBB), evita las técnicas de terapia génica que pueden introducir genes potencialmente dañinos en las células.
La nueva técnica, que pronto se pondrá a prueba como tratamiento en animales, también parece ser mucho más eficiente que otros métodos probados hasta la fecha, dicen los investigadores.
"Nuestros resultados establecen las bases para el desarrollo de terapias basadas en CMPi para el tratamiento de enfermedades genéticas devastadoras como la anemia de células falciformes", dice el investigador principal del estudio, Juan Carlos Izpisúa Belmonte, profesor de Salk en el Laboratorio de Expresión Génica.
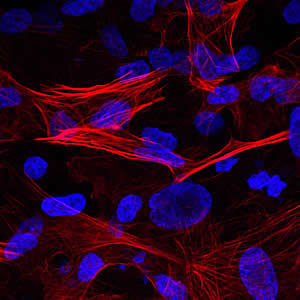
Los investigadores reprogramado células de piel tomadas de un paciente con la enfermedad de células falciformes para convertirlas en células madre pluripotentes inducidas (CMPi), las células inmaduras capaces de desarrollarse en cualquier tipo de tejido corporal.
Para asegurarse de que las células de la piel eran de hecho reprogramadas en células madre, los investigadores las indujeron para convertirse en células musculares, indicado por la presencia de protiens específicamente musculares (rojo) en la imagen. Los núcleos de las células --el compartimentos central que contienen el ADN-- se ven en color azul.
La enfermedad de células falciformes es un grupo de trastornos hereditarios en la sangre causada por mutaciones genéticas en el gen HBB, resultando en una hemoglobina anormal (la proteína que contiene hierro, que normalmente permite a las células de la sangre transportar el oxígeno). Esto hace que los glóbulos rojos sean duros y pegajosos y se asemejen a una "hoz" (herramienta de granja de forma curva). En los dos principales trastornos causados por mutaciones del gen HBB que son la anemia de células falciformes y la talasemia beta, las células rojas de la sangre no pueden transportar el oxígeno con eficacia.
Los síntomas de la enfermedad de células falciformes incluyen hinchazón de las manos y los pies, dolor debido a la obstrucción de los vasos sanguíneos, anemia y accidentes cerebrovasculares.
Los trastornos son más comunes entre las personas decendientes de África, el Mediterráneo y Oriente Medio. Uno de cada 500 afroamericanos y uno de cada 30.000 estadounidenses de origen hispano han nacido con enfermedad de células falciformes, según los Centros para el Control y Prevención de Enfermedades.
La enfermedad se puede curar con células madre o de médula ósea, pero hay un alto riesgo de que los receptores de trasplantes rechace la médula o las células donadas, lo cual puede resultar en efectos secundarios graves e incluso la muerte.
El equipo de investigadores de Salk, incluyendo a los coautores Mo Li y Keiichiro Suzuki, ambos socios de investigación en el laboratorio de Belmonte, se concentró en diseñar un método seguro para el uso de CMPi con el fin de corregir el gen HBB en pacientes que tienen copias defectuosas del gen.
Debido a que las CMPi vienen del propio cuerpo del paciente, el transplante tiene un menor riezgo de ser rechazado. Además, se han identiicado alrededor de 500 enfermedades causadas por mutaciones en el gen HBB, por lo que la corrección del gen podría curar un gran número de enfermedades relacionadas con el HBB en todo el mundo.
Sin embargo, las técnicas tradicionales generación de iPSC y terapia génica han demostrado ser potencialmente peligrosas, según los investigadores.
Muchos han utilizado virus para convertir células adultas en células madre e inducir a un gen normal de HBB para infectar y reparar células madre hematopoyéticas, las células madre que dan lugar a todas las células sanguíneas.
Pero cuando estas células madre reparadas son devueltas a los pacientes, pueden incluir transgenes (genes no deseados, que se han insertado en el genoma del huésped) y alterar la función normal del ADN. La técnica también es ineficiente, ya que corrigie sólo un pequeño porcentaje de mutaciones genéticas, y el éxito del trasplante ha demostrado ser poco frecuente en ensayos clínicos para el tratamiento de la talasemia beta.
"Queríamos corregir la mutación de tal manera que no dejara rastros no deseados en el genoma de un paciente", dice Suzuki.
Para ello, los investigadores utilizaron un método de dos pasos. En primer lugar, tomaron muestras de células adultas de la piel de un paciente con una mutación HBB que causa la anemia drepanocítica. Se utilizaron seis genes para lograr que estas células regresarlas a CMPi que podrían llegar a convertirse en células sanguíneas. Los genes fueron introducidos en las células mediante una técnica que evita el uso de virus y la inserción de los transgenes en el genoma de las células.
Su siguiente paso fue reparar la mutación del gen HBB en las células madre. Para cambiar el gen defectuoso por una copia normal en las CMPi, los investigadores usaron un adenovirus modificado (virus del resfriado común) que, a diferencia de los virus utilizados en otros métodos, no se replican en el cuerpo y no altera el ADN de la célula huésped. Los genes virales se han eliminado y reemplazado con una secuencia de ADN que contenía un gen normal HBB.
El virus modificado entregó el nuevo material genético en el interior de la CMPi, donde reemplazó la región de ADN que contiene el gen defectuoso con la secuencia que contiene el gen normal. "Esto sucede naturalmente, como sucede con una cremallera", dice Li. "El gen normal sólo se ajusta a la perfección, reemplazando al gen defectuoso".
Mediante la sustitución de una región relativamente grande de ADN, la técnica permite a los científicos reparar muchas mutaciones de genes a la vez, lo que sugiere que el método podría proporcionar una manera de tratar a cientos de tipos de enfermedades relacionadas con el HBB. La corrección de la mutación del gen HBB fue muy eficiente y el equipo de investigación ha llevado a cabo múltiples pruebas para asegurarse de que los genes errantes no se hayan integrado en el genoma.
Los científicos planean ahora hacer células de sangre obtenidas de células madre reparadas y poner a prueba su eficacia en animales. Si tiene éxito, esto podría conducir a terapias en seres humanos en donda las células madre del paciente se revietan en CMPi, entonces sean genéticamente reparadas y trasplantadas en la médula ósea del mismo paciente. Si tiene éxito, la médula ósea produce todas las nuevas células de la sangre, incluyendo una hemoglobina normal.
Fuente: Salk Institute, Diciembre 2011